-
×
 JETT BIO - Phân huỷ mùn bã hữu cơ, ổn định màu nước
1 × 579.000 ₫
JETT BIO - Phân huỷ mùn bã hữu cơ, ổn định màu nước
1 × 579.000 ₫ -
×
 NEOZYME - Enzyme giảm nhớt bạt, xử lý xác rong rêu, nhớt nước hiệu quả ao nuôi tôm
1 × 191.100 ₫
NEOZYME - Enzyme giảm nhớt bạt, xử lý xác rong rêu, nhớt nước hiệu quả ao nuôi tôm
1 × 191.100 ₫
Tổng số phụ: 770.100 ₫
Trong hóa học và đời sống công nghiệp, NH3 (hay còn gọi là Amoniac) là một trong những hợp chất vô cơ quan trọng nhất thế giới. Dù bạn nghe nói đến nó qua phân bón, chất tẩy rửa hay khí gas làm lạnh, việc hiểu rõ bản chất của NH3 là rất cần thiết để ứng dụng hiệu quả và an toàn.
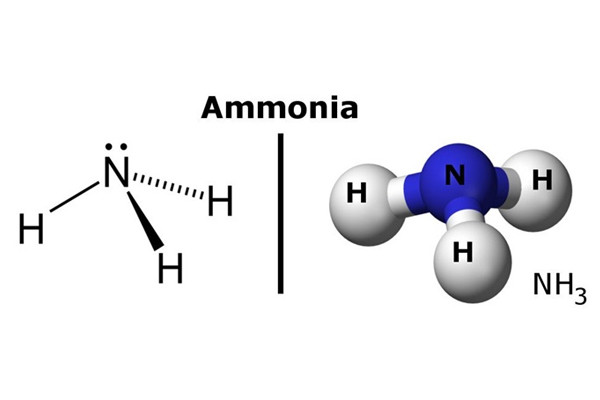
NH3 là công thức hóa học của Amoniac, một hợp chất vô cơ được cấu tạo từ 1 nguyên tử Nitơ (N) liên kết cộng hóa trị với 3 nguyên tử Hiđro (H). Đây là chất khí không màu, có mùi khai đặc trưng và tan rất nhiều trong nước.
Trong tự nhiên, Amoniac được sinh ra liên tục từ quá trình phân hủy các hợp chất hữu cơ có nguồn gốc từ động vật và thực vật (như nước tiểu, xác động vật) dưới tác động của các vi sinh vật trong đất.
Cấu tạo phân tử chi tiết:
Amoniac có tính chất vật lý nổi bật là mùi khai sốc, nhẹ hơn không khí và tan cực tốt trong nước. Về hóa học, NH3 thể hiện tính bazơ yếu và tính khử mạnh.
| Trạng thái | Chất khí không màu (ở điều kiện thường). |
| Mùi | Mùi khai và xốc rất đặc trưng (giống mùi nước tiểu lâu ngày). |
| Độ tan | Tan cực nhiều trong nước. 1 lít nước ở 20°C có thể hòa tan khoảng 800 lít khí NH3. |
| Tỷ trọng | Nhẹ hơn không khí (d ≈ 0.59), do đó khí NH3 thường bay lên cao. |
Amoniac có hai tính chất hóa học cơ bản cần lưu ý:
1. Tính Bazơ yếu:Khi tan trong nước, một phần nhỏ NH3 phản ứng tạo thành ion amoni (NH4+) và ion hydroxit (OH–), làm quỳ tím hóa xanh và dung dịch phenolphtalein hóa hồng.
NH3 + H2O ⇌ NH4+ + OH–
Tác dụng với axit: Tạo thành muối amoni (Hiện tượng “khói trắng” điển hình khi NH3 gặp hơi HCl).
NH3 + HCl → NH4Cl (Amoni clorua)
2. Tính khử:Trong phản ứng hóa học, Nitơ trong NH3 có số oxi hóa là -3 (thấp nhất), nên nó có xu hướng nhường electron để tăng số oxi hóa. Do đó, NH3 có thể tác dụng với Oxi (phản ứng cháy) hoặc các chất oxy hóa mạnh khác (như Clo).
Trong công nghiệp, phương pháp chủ yếu và hiệu quả nhất để sản xuất NH3 là quy trình Haber-Bosch, tổng hợp trực tiếp từ N2 và H2 ở nhiệt độ và áp suất cao.
Quy trình Haber-Bosch là nền tảng của ngành công nghiệp hóa chất hiện đại. Phản ứng diễn ra thuận nghịch và tỏa nhiệt:
Điều kiện tối ưu sản xuất hiện nay:
Sơ đồ quy trình tổng hợp Amoniac theo phương pháp Haber-Bosch
NH3 có vai trò sống còn trong nền kinh tế, với khoảng 80-85% sản lượng dùng để sản xuất phân đạm. Ngoài ra, nó là môi chất làm lạnh (R717) quan trọng và là nguyên liệu cho các ngành dệt may, thuốc nổ, tẩy rửa.
Theo số liệu thống kê mới nhất, sản lượng Amoniac toàn cầu đạt hơn 180 triệu tấn mỗi năm. Các ứng dụng chính bao gồm:
Đây là ứng dụng lớn nhất, tiêu thụ khoảng 80% sản lượng NH3 toàn cầu. Nó cung cấp nguồn Nitơ thiết yếu cho cây trồng dưới dạng:
Dung dịch Amoniac loãng (thường từ 5-10%) là “vua” trong việc tẩy rửa các vết bẩn cứng đầu:
NH3 là chất độc hại. Tiếp xúc trực tiếp có thể gây bỏng lạnh, mù lòa; hít phải nồng độ cao gây suy hô hấp và tử vong. Cần tuân thủ nghiêm ngặt quy tắc an toàn khi sử dụng.
Mặc dù hữu ích, NH3 là một “sát thủ vô hình” nếu rò rỉ:
NH3 (Amoniac) là một “con dao hai lưỡi”: vừa là nguyên liệu không thể thiếu để duy trì an ninh lương thực (phân bón) và công nghiệp toàn cầu, vừa là chất độc nguy hiểm cần sự thận trọng tối đa. Hiểu rõ NH3 là gì giúp chúng ta khai thác tối đa lợi ích kinh tế mà vẫn đảm bảo an toàn cho sức khỏe và môi trường.